Anlässlich des Jubiläums „100 Jahre Quantenphysik” im Jahr 2025 erschienen zahlreiche Beiträge in den Medien. Ein zentrales Anliegen der Quantenphysik war in den 1920er Jahren ein widerspruchsfreies Atommodell zu präsentieren. Dabei modifizierten Physiker das Bohrsche Atommodell und machten daraus das Orbitalmodell. Erstaunlich ist, dass das Bohrsche Atommodell als Atommodell der „klassischen Physik“ gilt, während das Orbitalmodell als Atommodell der Quantenphysik, also der „modernen Physik“, betrachtet wird.
Worin liegt nun der Unterschied? Oft wird angeführt, dass das Bohrsche Atommodell zwar falsch ist, sich aber gut für schulische Zwecke eignet. Bereits kurz nach der Veröffentlichung des Bohrschen Atommodells im Jahr 1913 wurde schon Kritik daran laut. Demnach müssten Elektronen auf Bahnen Energie abgeben und allmählich in den elektrisch positiven Atomkern stürzen. Alternativ müssten sich die elektrisch negativen Elektronen in der Atomhülle gegenseitig abstoßen. Eine Lösung des Problems schien dringend notwendig.
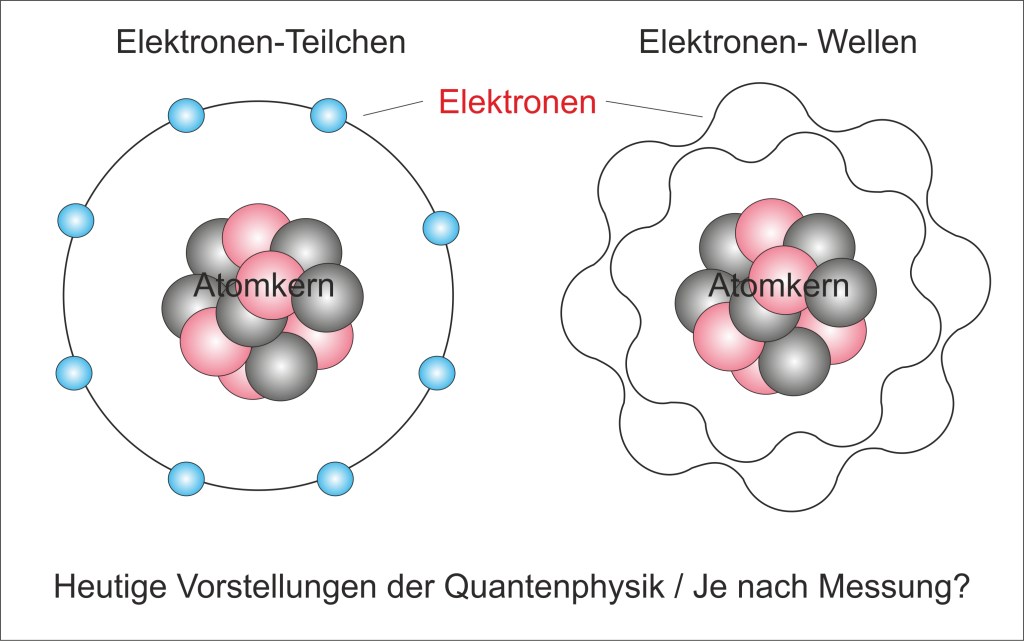
Niels Bohr, damals eine hoch anerkannte Persönlichkeit, setzte alles daran, eine Lösung zu finden. Am Ende stand das modifizierte Bohr-Sommerfeldsche Atommodell von 1916, das die Probleme jedoch auch nicht löste. Bereits mehr als ein Jahrzehnt zuvor hatten Max Planck und Albert Einstein Wärme- und Lichtwellen untersucht und Theorien entwickelt. De Broglie postulierte schließlich 1924 den sogenannten „Welle-Teilchen-Dualismus“. Wissenschaftler wie Werner Heisenberg, Erwin Schrödinger und Max Born die ebenfalls nach Lösungen suchten, begründeten 1925/1926 das Orbitalmodell. Grob gesagt stand am Ende der Bemühungen ein „Bohrsches Atommodell in Wellen“. Dieses „Orbitalmodell“ genannte Atommodell ist bis heute das von der Wissenschaft favorisierte Modell.
Doch stellt sich die Frage, ob es beim Orbitalmodell überhaupt gerechtfertigt ist, von einem neuen Atommodell und einer völlig neuen Physik zu sprechen. Auf jeden Fall nicht, wenn man vom Grundaufbau der Atommodelle ausgeht, der dem Rutherfordschen Atommodell von 1911 entspricht. Die Begründung, dass Teilchen je nach Messung auch Wellen sein können, erscheint etwas dürftig, um ein neues Atommodell und eine neue Physik auszurufen. Auch heute noch handelt es sich um ein Kern-Hülle-Atommodell mit einem positiv geladenen Atomkern im Zentrum und einer negativ geladenen Atomhülle. Diese Grundanordnung ist seit Rutherford unverändert, als sei dies die einzig mögliche Atomtheorie. Tatsächlich hätten spätestens seit der Entdeckung des Neutrons im Jahr 1932 auch andere Möglichkeiten berücksichtigt werden müssen.
Anstatt jedoch die wahrscheinlichste Lösung des Atomaufbaus aufzuzeigen, hängt die gesamte Atomphysik bis heute am Rutherfordschen und Bohrschen Atom-Grundaufbau fest, der über Jahrzehnte hinweg modifiziert wurde und immer noch inkonsistent ist. Oft wird mit experimentellen Messungen argumentiert, die das Orbitalmodell bestätigen sollen aber teilweise Zirkelschlüsse sind. Wie lange wird sich die Wissenschaft noch erlauben können, eine Physik zu verfolgen, die auf einer überholten Sicht des Atoms aufbaut? Unabhängig davon, ob Elektronen Wellen oder Teilchen sind, ist das Atommodell der Quantenphysik nicht haltbar. Das heutige Wissen über Protonen und Neutronen lässt nur einen Schluss über den Aufbau von Atomen zu: Ein schachbrettartiger Aufbau durch Protonen und Neutronen, ähnlich der Struktur von Ionenkristallen.





Hinterlasse einen Kommentar